Директни перорални антикоагуланти (ACOD): помощ за предписване в ежедневната практика
обобщение
Въведение
През последните години директните перорални антикоагуланти (ACOD) постепенно се въвеждат в ежедневната практика и представляват единствените антикоагуланти, алтернативни на витамин К (VKA), които могат да се прилагат през устата. За разлика от AVK, ACOD са директни и специфични инхибитори на един фактор на съсирване. Проведени са фаза III клинични изпитвания в областите на профилактика на венозна тромбоемболична болест (ВТЕ) при големи ортопедични операции, при лечение на ВТЕ, при вторична профилактика на рецидиви на ВТЕ и при предотвратяване на събития на ВТЕ. Артериални емболии при предсърдно мъждене ( AF). Като цяло тези проучвания показват, че ACOD са поне толкова ефективни, колкото стандартното лечение, със сходен или дори по-голям профил на безопасност по отношение на риска от кървене.
Признати индикации
ACODs са изследвани в множество клинични условия: профилактика на VTE при пациенти, хоспитализирани с остро медицинско състояние 1,2 или след тежка ортопедична хирургия, 3–15 лечение на остър VTE, 16–20 предотвратяване на рецидив. VTE, 17,21,22 предотвратяване на артериални тромбоемболични събития при AF, 23–26 и при остри коронарни синдроми (ACS) в комбинация с антитромбоцитни средства (APA). 27,28 Фаза III проучвания за превенция на ВТЕ при хоспитализирани медицински пациенти и при ОКС са разочароващи поради прекомерно висок процент на усложнения на кървенето. Следователно ACOD не са одобрени при тези показания. В Швейцария, молекулите и показанията, одобрени от SwissMedic, са в хронологичен ред:
Ривароксабан и апиксабан за профилактика на ВТЕ при голяма ортопедична хирургия.
Ривароксабан, дабигатран, апиксабан и едоксабан за лечение на ВТЕ.
Ривароксабан, дабигатран, апиксабан и едоксабан за вторична профилактика на рецидив на ВТЕ.
Дабигатран, ривароксабан, апиксабан и едоксабан за AF без увреждане на клапата.
Основни фармакокинетични свойства
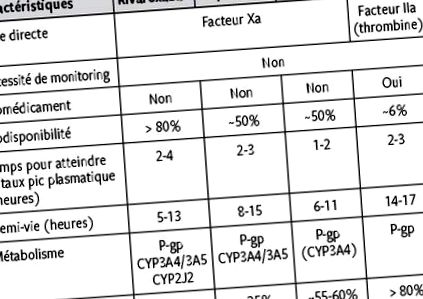
ACOD са директни и специфични инхибитори на един коагулационен фактор, като двете основни цели са фактор IIa и фактор Xa. Вече са публикувани множество статии с подробни описания на фармакокинетичните специфики на всеки ACOD. 29–31 Следователно в тази статия ще се съсредоточим само върху фармакологичните свойства, които имат най-голямо клинично значение и имат пряко въздействие върху предписването на тези лекарства (маса 1).
Някои фармакокинетични свойства са общи за всички ACOD. Първо, всички те имат бързо начало на действие след поглъщане през устата, като пиковите плазмени нива се достигат в рамките на 2 до 4 часа. Второ, всички те имат кратък полуживот, около 8 до 12 часа. Трето, за разлика от AVK, те не подлежат на взаимодействие с храната. Някои обаче трябва да се приемат по време на хранене, за да се подобри абсорбцията (вж. По-долу). Четвърто, лекарствените взаимодействия като цяло са по-малко клинично значими, отколкото при VKA, въпреки че това съобщение трябва да бъде по-нюансирано в някои ситуации. Основните неща, които трябва да имате предвид по отношение на взаимодействията, ще бъдат разгледани в специален раздел по-долу.
Някои важни фармакокинетични свойства се различават между ACOD. На първо място, бионаличността варира значително. Дабигатран е хидрофилна молекула, която не може да се абсорбира от храносмилателния тракт. Поради това се прилага като пролекарство, дабигатран ексилат, който има орална бионаличност 31–33. Докато някои автори се интересуват само от бъбречно елиминиране на активната форма на лекарството, други съобщават данни относно общото бъбречно елиминиране, включително активни и неактивни метаболити . В допълнение, дебатът все още продължава по следния въпрос: трябва ли да се има предвид процентът на бъбречно елиминиране на погълнатото лекарство или на абсорбираното активно лекарство? ?
Отново, за да опростим прагматичното послание, решихме да дадем приблизителни проценти на бъбречно елиминиране: над 80% за дабигатран, ≤ 60% за ксабани. Изглежда ни важно да настояваме за едно основно фундаментално послание: дабигатранът се елиминира в по-голямата си част от бъбреците, което не е случаят с ксабаните. За целите на тази статия задълбоченото обсъждане на по-фините различия (и дебати на мнения) относно процента на бъбречно елиминиране на различни ксабани изглеждаше напразно (маса 1).
Въвеждане на acod: дозировки
Дозите, предложени в таблица 2 всички са в строго съответствие с дозите, изследвани във фаза III проучвания, като единственото изключение е намалената доза дабигатран (2 х 110 mg дневно) при лечението и вторичната профилактика на ВТЕ при пациенти с умерена IR. Решихме да предложим тази доза, за да бъде в съответствие с дозите, препоръчани в Швейцарския сборник с лекарства за пациенти с повишен риск от кървене. Имайте предвид, че тази препоръка се основава единствено на фармакокинетични проучвания. 34
Показания за CEUS в съдовата медицина съгласно EFSUMB 2012 3
Препоръки за приемане и пренасочване с avk, хепарин и фондапаринукс
Ако пропуснете доза ACOD, предписана веднъж дневно, пропуснатата доза може да се приеме същия ден и след това да продължи лечението както обикновено на следващата сутрин. Пропуснатата доза не трябва да се приема на следващия ден (избягвайте двойна доза). За ACODs, предписани 2 пъти на ден, пропуснатата доза може да се приеме до 6 часа преди следващата планирана доза.
Преминаването от хепарин с ниско молекулно тегло (LMWH) към ACOD (или обратно) е относително лесно, тъй като двата антикоагуланта имат сходен фармакокинетичен профил. Първата доза ACOD трябва да се даде, когато нормално се очаква LMWH и обратно. Същата схема на реле се прилага и за фондапаринукс. За нефракциониран хепарин (UFH) трябва да се дава ACOD, когато инфузията на UFH се спре. За да преминете от ACOD към FNH, парентералният антикоагулант трябва да започне, когато е планирана дозата на ACOD. Трябва да се отбележи, че може да се наложи продължително забавяне между последната доза ACOD и началото на FNH в случай на RI. В допълнение, анализът на анти-Ха активността, провеждан за проследяване на лечението с UFH, може да бъде повлиян от остатъчната анти-Ха активност на ксабани (ривароксабан, апиксабан или едоксабан) в продължение на най-малко 24-36 часа след последната доза.
При преминаване от VKA към ACOD, първата доза ACOD може да се приеме веднага щом INR е ≤ 2,0, обикновено 24 до 72 часа след спиране на VKA, в зависимост от полуживота на AVK. В определени ситуации, когато тромботичният риск е висок (скорошно тромбоемболично събитие) и хеморагичният риск е нисък, може да се помисли да се даде първата доза ACOD, когато INR е 34 Преминаването от ACOD към VKA е по-проблематично, тъй като ACODs могат да повлияят резултата от INR. Ето защо, ние предлагаме да превключите за няколко дни с LMWH или fondaparinux, когато спирате ACOD и стартирате AVK след това. Ако няма история на тромбоемболично събитие (например при AF), AVK може да се стартира веднага след спиране на ACOD, без да се предава с LMWH или фондапаринукс.
Граници на заетостта
ACOD не са тествани при бременност и кърмене и при педиатрични пациенти. Следователно тяхното предписание е противопоказано при тези популации. Наличието на "чернодробно заболяване" също е критерий за изключване при проучвания фаза III, като определенията варират в различните проучвания. Препоръчваме да не се предписва ACOD при пациенти с чернодробна цироза на Child-Pugh B и C и \ или с необичайни чернодробни тестове (трансаминази ≥ 2 x горна граница на нормата) и \ или вторична коагулопатия до чернодробно увреждане.
ACODs са противопоказани при пациенти с тежка IR, като в по-голямата част от проучвания фаза III, граница на креатининов клирънс въз основа на оценка според формулата на Cockcroft-Gault (ClCr CG) 130 kg) е била много малко представена в клинични проучвания, които ето защо антикоагулацията с AVK изглежда по-разумна.
Странични ефекти
Присъщ "страничен ефект" на всяко лекарство за разреждане на кръвта е повишената склонност към кървене. В сравнение с VKA, ACOD има профил на безопасност, поне еквивалентен, ако не и по-добър, по отношение на хеморагичен риск и по отношение на това да станат пациенти в случай на хеморагично усложнение. 39 Рискът от вътречерепен кръвоизлив, който е едно от най-страховитите усложнения от кървене при всяка антикоагулантна терапия, постоянно се оказва по-нисък при ACOD, отколкото при VKA. Обърнете внимание, че ACODs са склонни да бъдат свързани със скромно, но значително увеличаване на риска от стомашно-чревно кървене 40 и необичайно маточно кървене. Поради това VKA понякога може да бъде предпочитан при пациенти с пептични язви или менометрорагия.
Общи нежелани реакции се съобщават за всички ACOD (гадене, свръхчувствителност и др.). Не всички потенциални странични ефекти, изброени в Компендиума, ще бъдат подробно описани тук, тъй като обсъждането на страничните ефекти, по-специфични за ACOD, изглежда по-полезно за целите на тази статия. Дабигатран е свързан със значителна честота на диспепсия (приблизително 10% от пациентите) и коремна болка (1–10% от пациентите), свързана с неговата дозировка. Ксабаните са свързани с по-висока честота на обрив и пруриго (1–10%) и повишени трансаминази (0,1–1%). Увеличението на трансаминазите обаче остава по-рядко, отколкото при стандартното лечение (еноксапарин и варфарин или само варфарин) в клинични проучвания. Съобщени са случаи на остра чернодробна недостатъчност за всички ACOD, но по-голямата част от пациентите са имали съпътстващи лекарства или заболявания, ограничаващи степента на сигурност на отчетността. 42
Клинично значими взаимодействия
Едно от основните предимства на ACOD пред VKA е намаляването на клинично значимите лекарствени взаимодействия. Намаляването на клинично значимите взаимодействия обаче не означава липса на всички взаимодействия.
Следователно има ли лекарства, чието едновременно предписване с ACOD трябва да бъде забранено? Имайки предвид метаболитните пътища, обсъдени по-горе, именно силните инхибитори и индуктори на CYP3A4 и \ или P-gp представляват лекарствата с потенциални взаимодействия с ACOD. Имайте предвид, че много лекарства, повлияващи CYP3A4, също действат върху P-gp. 43 Слабите или умерените инхибитори/индуктори на CYP3A4 теоретично могат да повлияят на плазмената концентрация на някои ACOD, но поради широкия терапевтичен прозорец на ACODs, изолираните взаимодействия от този тип не изглеждат клинично значими.
На практика комбинацията на дабигатран с някои инхибитори или индуктори на P-gp (хинидин, кетоконазол и др.) Е противопоказана и трябва да се избягва комбинацията с други лекарства, имащи значителен ефект върху функцията на P-gp (таблица 3). Също така, поради необходимостта от кисела среда за усвояване на дабигатран, инхибиторите на протонната помпа трябва да бъдат отстранени от приема на дабигатран.
- Терапевтични новини при хипертрофична кардиомиопатия - Swiss Medical Review
- Антитромботици при синдром на тромботични антифосфолипидни антитела - Медицински преглед
- Указ на Валонското правителство за създаване на схема за помощ за общините в рамките на благосъстоянието
- Перорални антикоагуланти Агенцията по лекарствата предупреждава за Previscan
- С деца - действия за предотвратяване на детското затлъстяване в училищата и столовите